紅磷P(s)和Cl2(g)發(fā)生反應(yīng)生成PCl3(g)和PCl5(g)。反應(yīng)過程和能量關(guān)系如圖所示(圖中的△H表示生成1mol產(chǎn)物的數(shù)據(jù))。
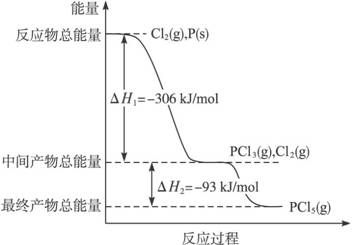
根據(jù)上圖回答下列問題:
(1)P和Cl2反應(yīng)生成PCl3的熱化學(xué)方程式是
�����;
(2)PCl5分解成PCl3和Cl2的熱化學(xué)方程式是
;
上述分解反應(yīng)是一個可逆反應(yīng)�����。溫度T1時�����,在密閉容器中加入0.80mol PCl5,反應(yīng)達(dá)平衡時PCl5還剩0.60 mol��,其分解率α1等于 �;若反應(yīng)溫度由T1升高到T2����,平衡時PCl5的分解率為α2,α2 α1(填“大于”�、“小于”或“等于”)����;
(3)工業(yè)上制備PCl5通常分兩步進(jìn)行�,先將P和Cl2反應(yīng)生成中間產(chǎn)物PCl3,然后降溫����,再和Cl2反應(yīng)生成PCl5。原因是________________________
(4)P和Cl2分兩步反應(yīng)生成1mol PCl5的△H3=____________����,P和Cl2一步反應(yīng)生成1molPCl5的△H4__________△H3(填“大于”、“小于”或“等于”)��。
(5)PCl5與足量水充分反應(yīng)����,最終生成兩種酸,其化學(xué)方程式是__________________________________���。